产品详情介绍
总览
美国Photosound公司生产的小动物光声断层扫描成像系统是一款无创三维成像平台。利用光声断层扫描成像技术对小动物成像,获取真实的高空间分辨率3D图像,成像对象包括:小鼠、体重小于200g的大鼠、离体组织、荧光探针样品等。单次扫描最快仅需36秒即可获取深层组织的3D图像,实现真正的三维光声成像。可在任意切面分析图像,包括横向解剖平面、矢状和冠状解剖平面以及不规则的解剖平面。横向解剖平面的空间分辨率150*150µm,矢状和冠状解剖平面分辨率150*230µm。分子成像灵敏度100 nM ICG。
光声成像结合了光学成像的高对比度和超声成像的深度穿透能力。小动物麻醉后浸入去离子水中,口鼻始终处于麻醉气体管路中维持麻醉状态,脉冲激光器生成特定波长的激光照射实验动物,动物体内特定的生物分子(如血红蛋白、黑色素、水、脂肪或外源性分子探针)吸收光能后被激发并转化为热能,导致局部温度升高和热弹性膨胀产生超声波,使用超声换能器检测超声波并转换为电信号,通过图像重建算法生成高分辨率的光声图像。
除3D解剖结构图谱外,TriTom小动物光声成像系统还可以对体内生理参数进行空间解析评估,例如体积血含量和氧合情况,无需注射造影剂。
TriTom 成像平台适用于临床前研究,包括肿瘤、毒理学、发育生物学、组织工程和再生、神经科学、心血管成像,以及药物、疗法和光学和荧光成像探针的开发。
产品特征
光声激发波长范围532nm & 650-1320nm,涵盖可见光,NIR I 和 NIR II 激发光源
大体积光声断层扫描成像,可在任意切面分析成像对象
单次扫描最快仅需36 秒,具有出色的分子灵敏度
1nm的激光调谐分辨率,单次扫描可设置15个以上的激发波长扫描顺序
扫描对象包括:造影剂微量比色皿管,离体组织,小鼠
集成气体麻醉管线和可调节小鼠支架,操作方便,可重复进行体内纵向研究
单次扫描可评估多个造影剂样本(50 µL 或更少体积),加速造影剂开发,避免浪费
用户友好的集成软件,旨在最大限度地缩短实验时间,并在几秒钟内重建大规模体积
开放数据格式,允许使用第三方软件进行图像重建和数据管理

应用案例
小鼠肿瘤组织监测:
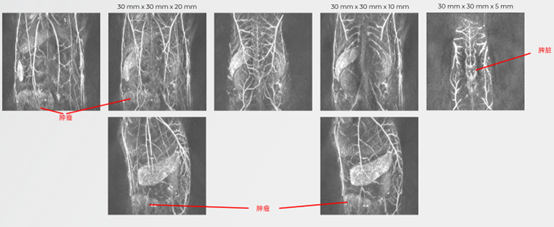
无标记的小鼠肿瘤组织成像
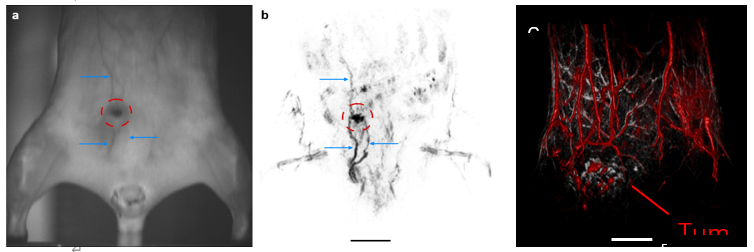
无毛小鼠(左)和 nu/nu 小鼠(右)中的人类乳腺癌异种移植(BT474 细胞)。(a、b)显示了相机观察结果和相应的冠状 MIP 板,由 700 nm 和 1064 nm 激光激发获得的 TriTom 图像构建而成。蓝色箭头和红色 ROI 表示高分辨率图像中可见的浅表血管特征和肿瘤环境。(c)复合皮肤(532 nm;灰色)和深层组织(890 nm;红色)3D 图像。肿瘤大小 = 10.6 x 4.7 x 11.6 mm3
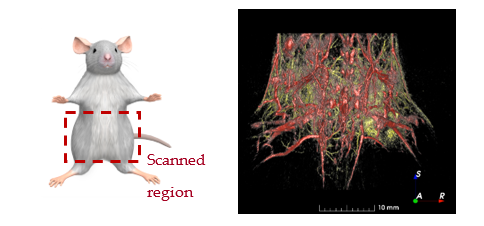
转移性乳腺癌活体小鼠模型中的深层和浅表血管 TriTom 复合图像
红色 – 深层血管(890 nm 激发)
黄色 – 浅层血管(532 nm 激发)
ICG & 血红蛋白光声分子解离成像
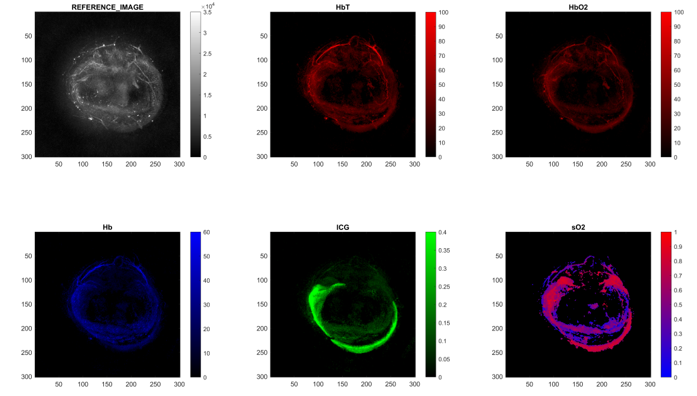
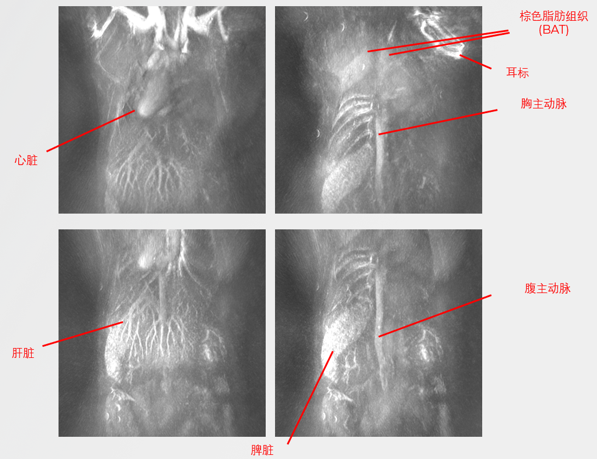
无标记小鼠血管成像
神经成像
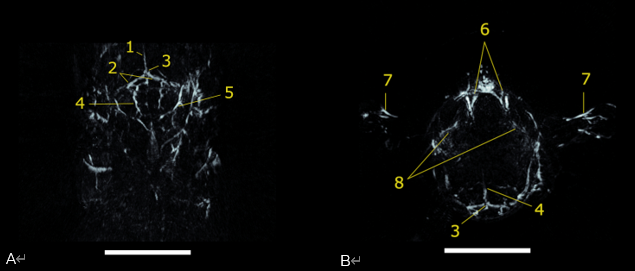
10 毫米厚的 (A) 冠状和 (B) 横向最大强度投影板,从 750 nm 扫描重建 PAI 体积。1) 上矢状窦,2) 横窦,3) 窦汇合处,4) 脑动脉,5) 耳动脉,6) 颈静脉,7) 肱动脉,8) 眼动脉。比例尺为 5 毫米。
造影剂开发
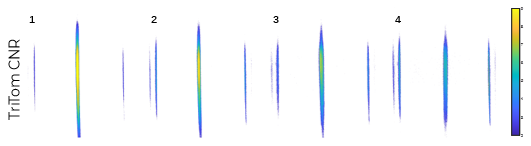
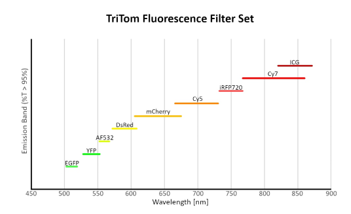
参考文献
I. B. Belyaev et al., "Laser-Synthesized Germanium Nanoparticles as Biodearadable Material for Near.Infrared Photoacoustic lmaging and Cancer Phototherapy," AdvSci 2307060, 2024, doi: 10.1002/advs.202307060.
R. M. Cam, C. Wang, w. Thompson, S. A. Ermilov, M. A. Anastasio, and u. Villa, "Spatiotemporal lmageReconstruction to Enable High-Frame Rate Dynamic Photoacoustic Tomography with Rotating-Gantry Volumetric lmagers," ArXiv, 2023, doi: 10.48550/arXiv.2310.00529.
K. Huda, D. J. Lawrence, w. Thompson, S. H. Lindsey, and C. L. Bayer, "in vivo noninvasive systemicmyography of acute systemic vasoactivity in female pregnant mice," Nature Communications, vol14,no.1,2023,doi: 10.1038/s41467-023-42041-8.
V. D. Vincely and C. L. Bayer, "Functional photoacoustic imaging for placental monitoring: A minireview," lEEE Transactions on Ultrasonics, Ferroelectrics, and Frequency Control, pp. 1-1, 2023, doi.10.1109/tuffc.2023.3263361.
W. R. Thompson et al., "Characterizing a photoacoustic and fluorescence imaging platform forpreclinical murine longitudinal studies," 1. Biomed. Opt, vol. 28, no. 3, p. 036001, 2023, doi:10.1117/1.JBO.28.3.036001.
M. Delcroix, A. Reddy Marri, S. Parant, P. C. Gros, and M. Bouché, "Water-soluble Fe(l) complexes fortheranostic application: Synthesis, photoacoustic imaging and photothermal conversion," Eur. ..Inorg.Chem,, vol.26, no.27,2023, doi: 10.1002/eiic.202300138.
S. Singh et al., "Size-tunable lCG-based contrast agent platform for targeted near-infraredphotoacoustic imaging," Photoacoustics, vol. 29, p.100437, 2023, doi: 10.1016/i.pacs.2022.100437
Z. Zhao, c. B. Swartchick, and J. Chan, "Targeted contrast agents and activatable probes forphotoacoustic imaging of cancer," Chem Soc Rev, vol. 5l, no.3, pp. 829-868, 2022, doi.10.1039/d0cs00771d.
J. Kim, A. M. Yu, K. P. Kubelick, and S. Y. Emelianov, "Gold nanoparticles conjugated with DNAaptamer for photoacoustic detection of human matrix metalloproteinase-9," Photoacoustics, vol. 25p.100307, 2022, doi: 10.1016/i.pacs.2021.100307.
M. R. Chetyrkina et al., "Carbon Nanotube Microscale Fiber Grid as an Advanced Calibration Systemfor Multispectral Optoacoustic lmaging," Acs Photonics, vol. 9, no.10, pp. 3429-3439, 2022, doi:10.1021/acsphotonics.2c01074.
M. D. Mokrousov et al, "indocyanine green dye based bimodal contrast agent tested byphotoacoustic/fluorescence tomography setup," Biomed. Opt. Express, vol. 12, no. 6, p. 3181, 2021, doi.10.1364/boe.419461.
A. Juronis and M. Jasinskas, "Breakthrough instruments and products PhotoSonus M+ laser forphotoacoustic imaging," Review of Scientific instruments, vol. 92, no. 5, p. 059502, 2021, doi.10.1063/5.0053559.
K. Huda, c. wu, J. G. Sider, and c. L, Baver, "Spherical-view photoacoustic tomography for monitoringin vivo placental function," Photoacoustics, vol. 20,p.100209, 2020, doi: 10.1016/i.pacs.2020.100209
E. M. Donnelly, K. P. Kubelick, D.s. Dumani, and S. Y. Emelianov, "Photoacoustic lmage-GuidedDelivery of Plasmonic-Nanoparticle-Labeled Mesenchymal Stem Cells to the Spinal Cord," NanoLetters, vol.18, no.10, pp.6625-6632,2018, doi: 10.1021/acs.nanolett.8b03305


